
前列腺癌症(PCa)是一种令人沮丧的免疫原性“冷”肿瘤,通常在临床上无法获得令人满意的免疫治疗结果。焦亡是一种免疫原性细胞死亡形式,可以有效激活抗肿瘤免疫反应,促进细胞毒性T淋巴细胞浸润,并将肿瘤从“冷”转化为“热”。然而,焦亡药物的体内应用依然受到严重限制,同时光免疫疗法引起的肿瘤PD-L1的上调也进一步促进了免疫逃逸的发生。苏州大学Weijie Zhang、李盛亮和Jianquan Hou开发了一种新型的pH响应性纳米光敏剂(YBS-BMS NPs-RKC),其具有结合免疫原性焦亡诱导和免疫检查点阻断的能力。
本文要点
(1)研究将配备有细胞膜锚定肽RKC的pH响应性聚合物用作载体,并进一步包载近红外活化的半导体聚合物光敏剂YBS和PD-1/PD-L1复合物小分子抑制剂BMS-202。
(2)YBS-BMS NPs-RKC具有pH驱动的膜锚定和激活焦亡的能力。体外和体内研究表明,这种双管齐下的疗法可刺激强大的抗肿瘤免疫反应,抑制原发性肿瘤进展,并唤起长期免疫记忆,抑制肿瘤复发和转移。这项工作为前列腺癌免疫治疗提供了一个有效的自协同平台,并为开发更具生物相容性的光控焦亡诱导剂提供了新的思路。
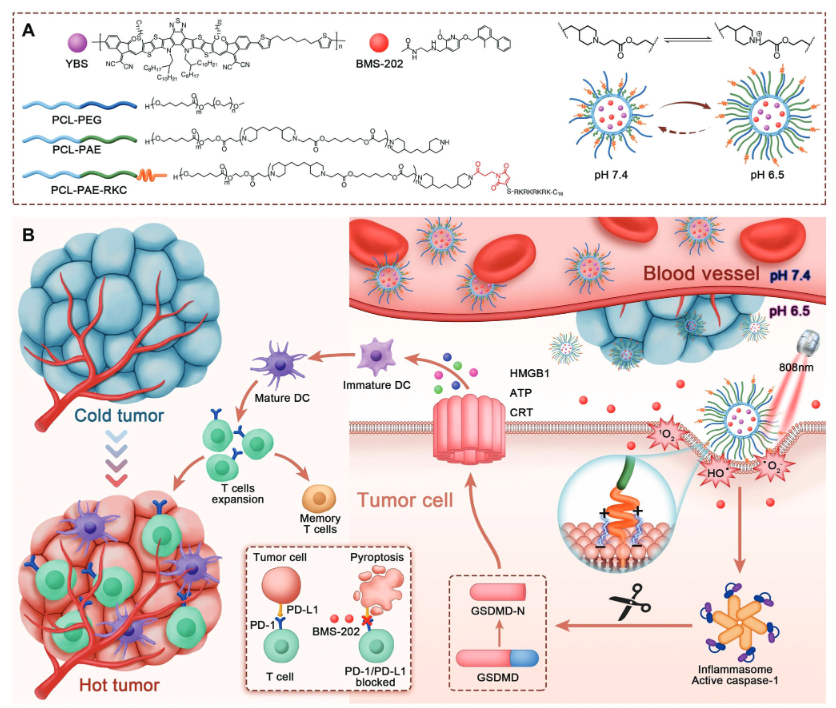
He Wang, et al. Dual-Pronged Attack: pH-Driven Membrane-Anchored NIR Dual-Type Nano-Photosensitizer Excites Immunogenic Pyroptosis and Sequester Immune Checkpoint for Enhanced Prostate Cancer Photo-Immunotherapy. Advanced Science. 2023
DOI:10.1002/advs.202302422
https://onlinelibrary.wiley.com/doi/10.1002/advs.202302422


















