ACS Nano:利用纳米复合水凝胶捕获和利用miRNAs以重塑效应T细胞和调节性T细胞增强光热免疫治疗
 柚子
柚子
在恶性肿瘤的免疫治疗过程中,效应T细胞和调节性T细胞(Tregs)之间的平衡失调以及个体差异导致的疗效不确定是两个亟待解决的问题。有鉴于此,西安交通大学陈鑫教授和张彦民教授设计了一种可注射的纳米复合水凝胶系统(SNAs@M-Gel),其能够通过刺激反应性调节多种肿瘤相关microRNA抑制Treg增殖,并有效阻断PD-1/PD-L1介导的免疫逃避。
本文要点:
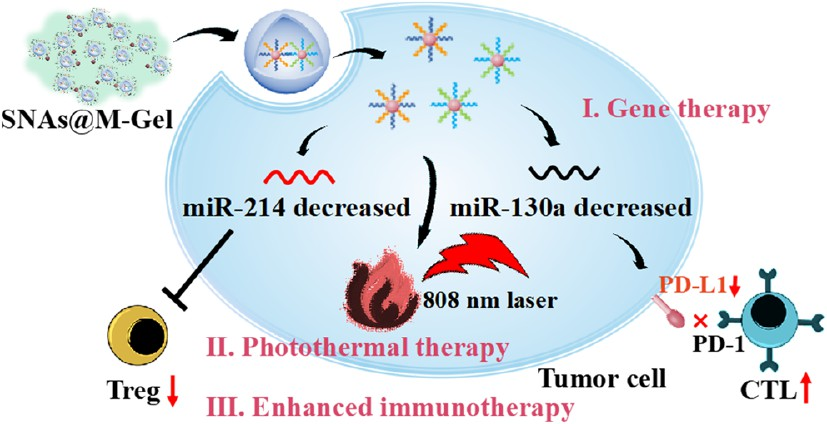
(1)该系统能够实现依赖于microRNA的光热免疫治疗,是一种高效、个性化的肿瘤治疗方法。实验以氧化海藻酸钠(OSA)和癌细胞膜(CCM)包封的球形核酸纳米粒子(SNAs@M)作为前体,利用对pH敏感的席夫碱键的形成和内源性钙离子(Ca2+)交联在肿瘤部位原位构建了SNAs@M-Gel水凝胶。在治疗期间,SNAs@M-Gel可在局部长期保留(长达10天),并将SNAs@M纳米颗粒连续释放到肿瘤微环境中。研究发现,SNAs@M可通过CCM的靶向能力精准进入肿瘤细胞,并与过表达的miR-214和miR-130a发生特异性杂交,导致肿瘤细胞上的PD-L1表达显著下调,恢复被Tregs抑制的细胞毒性T淋巴细胞(CTL)的功能,实现免疫微环境重塑。
(2)此外,作为交联剂的miRNAs也能够促进SNAs的聚集,直接促进光热制剂在肿瘤细胞内的局部产生,进而可以在近红外(NIR)照射下实现具有高选择性的光热治疗。实验结果表明,这一系列事件不仅会破坏原发肿瘤,还能够诱导大量肿瘤相关抗原的释放,以触发邻近树突状细胞(DCs)的成熟和肿瘤特异性CTLs的启动,并同时消耗Tregs,以逆转促肿瘤免疫微环境,增强光热免疫疗法的整体治疗效果。
Li Chen. et al. Remodeling of Effector and Regulatory T Cells by Capture and Utilization of miRNAs Using Nanocomposite Hydrogel for Tumor-Specific Photothermal Immunotherapy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c18801
https://pubs.acs.org/doi/10.1021/acsnano.4c18801
版权声明:
本平台根据相关科技华体汇下注平台 电竞投注官网 、教材以及网站编译整理的内容,仅用于对相关科学作品的介绍、评论以及课堂教学或科学研究,不得作为商业用途。


